Коэнзим Q - цитохром с редуктаза - Coenzyme Q – cytochrome c reductase
| UCR_TM | |||||||||
|---|---|---|---|---|---|---|---|---|---|
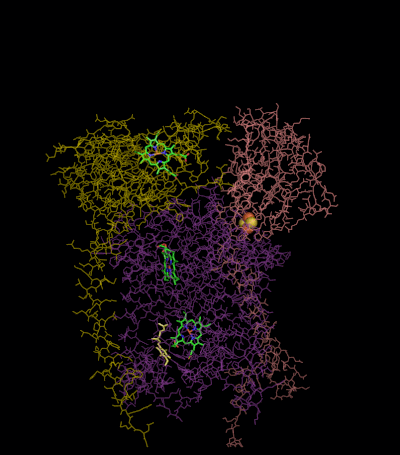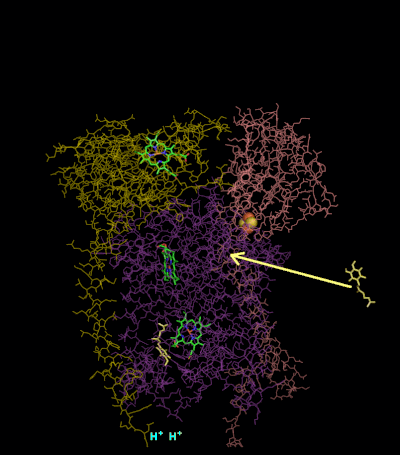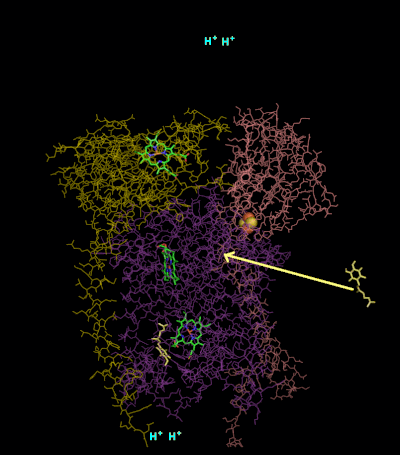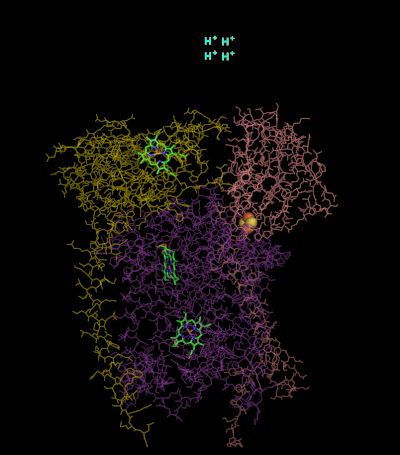
 Кристаллическая структура митохондриального комплекса цитохрома bc, связанного с убихиноном .
| |||||||||
| Идентификаторы | |||||||||
| Символ | UCR_TM | ||||||||
| Pfam | PF02921 | ||||||||
| ИнтерПро | IPR004192 | ||||||||
| SCOP2 | 1be3 / SCOPe / SUPFAM | ||||||||
| TCDB | 3.D.3 | ||||||||
| OPM суперсемейство | 92 | ||||||||
| Белок OPM | 3cx5 | ||||||||
| Мембранома | 258 | ||||||||
| |||||||||
| убихинол — цитохром-с редуктаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| ЕС нет. | 7.1.1.8 | ||||||||
| № CAS | 9027-03-6 | ||||||||
| Базы данных | |||||||||
| IntEnz | Просмотр IntEnz | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | Просмотр NiceZyme | ||||||||
| КЕГГ | Запись в KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| ПРИАМ | профиль | ||||||||
| Структуры PDB | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | Amigo / QuickGO | ||||||||
| |||||||||
Коэнзим Q: цитохром с - оксидоредуктазами , иногда называют цитохром Ьсом 1 комплекс , а в другое время сложного III , третий комплекс в цепи переноса электронов ( EC 1.10.2.2 ), играет важную роль в биохимической генерации АТФ ( окислительное фосфорилирование ). Комплекс III представляет собой мультисубъединичный трансмембранный белок, кодируемый как митохондриальным ( цитохромом b ), так и ядерным геномами (всеми другими субъединицами). Комплекс III присутствует в митохондриях всех животных и всех аэробных эукариот, а также во внутренних мембранах большинства эубактерий . Мутации в Комплексе III вызывают непереносимость физических упражнений, а также мультисистемные нарушения. BC1 комплекс содержит 11 субъединиц, 3 респираторных субъединиц (цитохром B, цитохром C1, Rieske белок), 2 основных белки и 6 веса низкомолекулярных белков .
Убихинол - цитохром-с-редуктаза катализирует химическую реакцию
- QH 2 + 2 феррицитохрома c Q + 2 ферроцитохрома c + 2 H +
Таким образом, двумя субстратами этого фермента являются хинол (QH 2 ) и ферри- (Fe 3+ ) цитохром c , тогда как его тремя продуктами являются хинон (Q), ферро- (Fe 2+ ) цитохром c и H + .
Этот фермент принадлежит к семейству оксидоредуктаз , в частности тех, которые действуют на дифенолы и родственные вещества в качестве донора с цитохромом в качестве акцептора. Этот фермент участвует в окислительном фосфорилировании . Он имеет четыре кофактора : цитохром c 1 , цитохром b-562, цитохром b-566 и ферредоксин 2-железа типа Риске .
Номенклатура
Систематическое название данного фермента класс убихинол: феррицитохром с оксидоредуктазами . Другие широко используемые имена включают:
|
|
Состав
По сравнению с другими основными субъединицами цепи переноса электронов, перекачивающими протоны , количество обнаруженных субъединиц может быть небольшим, вплоть до трех полипептидных цепей. Это число действительно увеличивается, и у высших животных обнаружено одиннадцать субъединиц. Три субъединицы имеют протезные группы . Цитохрома Ь субъединица имеет два б -тип гемов ( б л и б Н ), цитохром с субъединицей имеет один с -типом гем ( с 1 ), а Rieske железа Серы белковая субъединица (ISP) , имеет два железа, серу , два железо-серный кластер (2Fe • 2S).
Структуры комплекса III: PDB : 1KYO , PDB : 1L0L
Состав комплекса
У позвоночных комплекс bc 1 или Комплекс III содержит 11 субъединиц: 3 респираторные субъединицы, 2 коровых белка и 6 низкомолекулярных белков. Протеобактериальные комплексы могут содержать всего три субъединицы.
Таблица субъединичного состава комплекса III
| Нет. | Название подразделения | Человеческий белок | Описание протеина от UniProt | Семейство pfam с человеческим белком |
|---|---|---|---|---|
| Белки респираторной субъединицы | ||||
| 1 | MT-CYB / Cyt b | CYB_HUMAN | Цитохром b | Pfam PF13631 |
| 2 | CYC1 / Cyt c1 | CY1_HUMAN | Цитохром c1, гем-белок, митохондриальный | Pfam PF02167 |
| 3 | Rieske / UCR1 | UCRI_HUMAN | Субъединица комплекса цитохрома b-c1 Риске, митохондриальная ЭК 1.10.2.2 | Pfam PF02921 , Pfam PF00355 |
| Субъединицы основного белка | ||||
| 4 | QCR1 / SU1 | QCR1_HUMAN | Субъединица 1 комплекса цитохрома b-c1, митохондриальная | Pfam PF00675 , Pfam PF05193 |
| 5 | QCR2 / SU2 | QCR2_HUMAN | Субъединица 2 комплекса цитохрома b-c1, митохондриальная | Pfam PF00675 , Pfam PF05193 |
| Белковые субъединицы с низкой молекулярной массой | ||||
| 6 | QCR6 / SU6 | QCR6_HUMAN | Субъединица 6 комплекса цитохрома b-c1, митохондриальная | Pfam PF02320 |
| 7 | QCR7 / SU7 | QCR7_HUMAN | Субъединица 7 комплекса цитохрома b-c1 | Pfam PF02271 |
| 8 | QCR8 / SU8 | QCR8_HUMAN | Субъединица 8 комплекса цитохрома b-c1 | Pfam PF02939 |
| 9 | QCR9 / SU9 / UCRC | QCR9_HUMAN а | Субъединица 9 комплекса цитохрома b-c1 | Pfam PF09165 |
| 10 | QCR10 / SU10 | QCR10_HUMAN | Субъединица 10 комплекса цитохрома b-c1 | Pfam PF05365 |
| 11 | QCR11 / SU11 | QCR11_HUMAN | Субъединица 11 комплекса цитохрома b-c1 | Pfam PF08997 |
- а У позвоночных продукт расщепления 8 кДа от N-конца белка Rieske ( сигнальный пептид ) сохраняется в комплексе как субъединица 9. Таким образом, субъединицы 10 и 11 соответствуют грибковым QCR9p и QCR10p.
Реакция
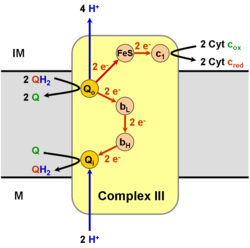
Он катализирует восстановление цитохрома с за счет окисления кофермента Q (CoQ) и сопутствующей перекачки 4 протонов из митохондриального матрикса в межмембранное пространство:
- QH 2 + 2 цитохрома c (Fe III ) + 2 H+
в→ Q + 2 цитохрома c (Fe II ) + 4 H+
вне
В процессе, называемом Q-циклом , два протона потребляются из матрицы (M), четыре протона высвобождаются в межмембранное пространство (IM), а два электрона передаются цитохрому c .
Механизм реакции
Механизм реакции для комплекса III (цитохром bc1, кофермент Q: цитохром С оксидоредуктаза) известен как цикл убихинона («Q»). В этом цикле четыре протона высвобождаются в положительную сторону «P» (межмембранное пространство), но только два протона захватываются с отрицательной стороны «N» (матрица). В результате на мембране образуется протонный градиент . В общей реакции два убихинола окисляются до убихинонов, а один убихинон восстанавливается до убихинола . В полном механизме два электрона передаются от убихинола к убихинону через два промежуточных продукта цитохрома с.
В целом :
- 2 x QH 2 окисляется до Q
- 1 x Q уменьшен до QH 2
- 2 x Cyt c уменьшен
- 4 x H + высвобождается в межмембранное пространство
- 2 x H + взяты из матрицы
Реакция протекает в соответствии со следующими этапами:
1 тур :
- Цитохром b связывает убихинол и убихинон.
- Центр 2Fe / 2S и гем B L каждый оттягивают электрон от связанного убихинола, высвобождая два атома водорода в межмембранное пространство.
- Один электрон переходит к цитохрома с 1 от центра 2Fe / 2S, в то время как другая передается от B L гема к B H гема.
- Цитохром c 1 передает свой электрон цитохрому c (не путать с цитохромом c1), а гем B H передает свой электрон соседнему убихинону, что приводит к образованию убисемихинона.
- Цитохром c диффундирует. Первый убихинол (теперь окисленный до убихинона) высвобождается, в то время как семихинон остается связанным.
2 тур :
- Второй убихинол связывается цитохромом b.
- Центр 2Fe / 2S и гем B L каждый оттягивают электрон от связанного убихинола, высвобождая два атома водорода в межмембранное пространство.
- Один электрон переходит к цитохрома с 1 от центра 2Fe / 2S, в то время как другая передается от B L гема к B H гема.
- Цитокром c 1 затем передает свой электрон цитохрому c , в то время как соседний семихинон, произведенный в первом раунде, забирает второй электрон из гема B H вместе с двумя протонами из матрицы.
- Второй убихинол (теперь окисленный до убихинона) вместе с вновь образованным убихинолом высвобождается.
Ингибиторы комплекса III
Есть три отдельные группы ингибиторов Комплекса III.
- Антимицин А связывается с сайтом Q i и ингибирует перенос электронов в Комплексе III от гема b H к окисленному Q (ингибитор сайта Qi).
-
Миксотиазол и стигмателлин связывается с Q ö сайта и ингибирует перенос электронов от восстановленного QH 2 с белком серы Rieske железа. Миксотиазол и стигмателлин связываются с отдельными, но перекрывающимися карманами внутри сайта Q o .
- Миксотиазол связывается ближе к цитохрому bL (отсюда его называют « проксимальным » ингибитором).
- Стигмателлин связывается дальше от гема bL и ближе к белку серы Rieske Iron, с которым он сильно взаимодействует.
Некоторые из них были коммерциализированы как фунгициды ( производные стробилурина , наиболее известным из которых является азоксистробин ; ингибиторы QoI ) и как противомалярийные средства ( атоваквон ).
Также пропилгекседрин подавляет цитохром с редуктазу.
Свободные кислородные радикалы
Небольшая часть электронов покидает цепь переноса электронов, не достигнув комплекса IV . Преждевременная утечка электронов к кислороду приводит к образованию супероксида . Актуальность этой второстепенной побочной реакции заключается в том, что супероксид и другие активные формы кислорода очень токсичны и, как считается, играют роль в нескольких патологиях, а также в старении ( свободнорадикальная теория старения ). Утечка электронов происходит главным образом на Q O сайта и стимулируется антимицин А . Антимицина А блокирует б гемов в восстановленном состоянии, предотвращая их повторное окисление на Q я сайт, который, в свою очередь, вызывает стационарные концентраций Q о семихинонных расти, последний вид , реагирующий с кислородом с образованием супероксида . Считается, что эффект высокого мембранного потенциала имеет аналогичный эффект. Супероксид, продуцируемый в сайте Qo, может высвобождаться как в митохондриальный матрикс, так и в межмембранное пространство, где затем может достигать цитозоля. Это можно объяснить тем фактом, что Комплекс III может производить супероксид в виде проницаемого для мембраны HOO •, а не в виде проницаемого для мембраны O-.
2.
Названия генов человека
MT-CYB : цитохром b, кодируемый мтДНК ; мутации, связанные с непереносимостью физических упражнений
CYC1 : цитохром c1
CYCS : цитохром c
UQCRFS1 : железо-серный белок Риске
UQCRB : убихинон- связывающий белок, мутация, связанная с дефицитом митохондриального комплекса III ядерного типа 3
UQCRH : шарнирный белок
UQCRC2 : Core 2, мутации, связанные с дефицитом митохондриального комплекса III, ядерный тип 5
UQCRC1 : Ядро 1
UQCR : субъединица 6.4KD
UQCR10 : субъединица 7.2KD
TTC19 : недавно идентифицированная субъединица, мутации, связанные с дефицитом комплекса III ядерного типа 2.
Мутации в генах комплекса III при болезнях человека
Мутации в генах, связанных с комплексом III, обычно проявляются непереносимостью физических упражнений. Сообщалось, что другие мутации вызывают септооптическую дисплазию и мультисистемные расстройства. Тем не менее, мутации в BCS1L , ген отвечает за правильное созревание комплекса III, может привести к синдрому Bjørnstad и синдром грацильного , который у новорожденных являются летальными условиями , которые имеют Multisystem и неврологические проявления типизации тяжелые митохондриальные расстройств. Патогенность нескольких мутаций была подтверждена на модельных системах, таких как дрожжи.
Степень, в которой эти различные патологии вызваны биоэнергетическим дефицитом или перепроизводством супероксида, в настоящее время неизвестна.
Смотрите также
Дополнительные изображения
Рекомендации
дальнейшее чтение
- Маррес CM, Слейтер EC (1977). «Полипептидный состав очищенного QH2: цитохром с оксидоредуктаза из митохондрий говяжьего сердца». Биохим. Биофиз. Acta . 462 (3): 531–548. DOI : 10.1016 / 0005-2728 (77) 90099-8 . PMID 597492 .
- Rieske JS (1976). «Состав, структура и функции комплекса III дыхательной цепи». Биохим. Биофиз. Acta . 456 (2): 195–247. DOI : 10.1016 / 0304-4173 (76) 90012-4 . PMID 788795 .
- Викстром М., Краб К., Сарасте М. (1981). «Протон-переносящие цитохромные комплексы». Анну. Rev. Biochem . 50 : 623–655. DOI : 10.1146 / annurev.bi.50.070181.003203 . PMID 6267990 .
Внешние ссылки
- сайт комплекса цитохрома bc 1 (Эдвард А. Берри) в Wayback Machine (архив 9 октября 2006 г.) на lbl.gov
- комплексный сайт цитохрома bc 1 (Энтони Р. Крофтс) на uiuc.edu
- PROMISE База данных: цитохром Ьс 1 комплекс в archive.today ( в архиве 27 августа 1999) в scripps.edu
- Интерактивная молекулярная модель комплекса III в машине обратного пути (архивировано 12 января 2009 г.) (требуется MDL Chime )
- UMich Ориентация белков в мембранах семейства / суперсемейство-3 - Расчетные положения bc1 и родственных комплексов в мембранах
- Коэнзим + Q-цитохром-с + редуктаза в Национальных медицинских предметных рубриках США (MeSH)