Фторид кобальта (II) - Cobalt(II) fluoride
|
|
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Фторид кобальта (II)
|
|
| Другие названия
дифторид кобальта
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard |
100.030.044 |
| Номер ЕС | |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| Co F 2 | |
| Молярная масса | 96,93 г / моль |
| Появление | Красное кристаллическое твердое вещество |
| Плотность | 4,46 г / см 3 (безводный) 2,22 г / см 3 (тетрагидрат) |
| Температура плавления | 1217 ° С (2223 ° F, 1490 К) |
| Точка кипения | 1400 ° С (2550 ° F, 1670 К) |
| 1,4 г / 100 мл (25 ° С) | |
| Растворимость | растворим в HF нерастворим в спирте , эфире , бензоле |
| + 9490,0 · 10 −6 см 3 / моль | |
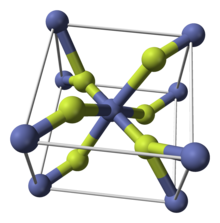
| Состав | |
| тетрагональный (водный) орторомбический (тетрагидрат) |
|
| Опасности | |
| NFPA 704 (огненный алмаз) | |
| Смертельная доза или концентрация (LD, LC): | |
|
LD 50 ( средняя доза )
|
перорально (крыса): 150 мг / кг |
| Родственные соединения | |
|
Другие анионы
|
оксид кобальта (II) , , кобальта хлорид (II) , |
|
Другие катионы
|
железа (II) , фторид , никель фторид (II) , |
|
Родственные соединения
|
трифторид кобальта |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Фторид кобальта (II) представляет собой химическое соединение с формулой (CoF 2 ). Это розовое кристаллическое твердое соединение, которое является антиферромагнитным при низких температурах (T N = 37,7 K). Формула дана как для красного тетрагонального кристалла (CoF 2 ), так и для тетрагидратного красного ортогонального кристалла (CoF 2 · 4H 2 O ). CoF 2 используется в чувствительных к кислороду областях, а именно в производстве металлов. В низких концентрациях он используется в здравоохранении. CoF 2 плохо растворяется в воде. Соединение можно растворить в теплой минеральной кислоте и разложить в кипящей воде. Тем не менее, гидрат является водорастворимым, особенно дигидрат CoF 2 · 2H 2 O и тригидрат CoF 2 · 3H 2 O формы соединения. Гидрат также разлагается при нагревании.
Подготовка
Фторид кобальта (II) может быть получен из безводного хлорида кобальта (II) или оксида кобальта (II) в потоке фтороводорода :
- CoCl 2 + 2HF → CoF 2 + 2HCl
- CoO + 2HF → CoF 2 + H 2 O
Он образуется при реакции фторида кобальта (III) с водой.
Тетрагидрат кобальта фторид (II) , образуется путем растворения кобальта (II) в плавиковой кислоте. Безводный фторид можно извлечь из него дегидратацией . Другой синтез может происходить при более высоких температурах. Было показано, что при 500 ° C фтор соединяется с кобальтом, образуя смесь CoF 2 и CoF 3 .
Использует
Фторид кобальта (II) можно использовать в качестве катализатора для легирования металлов. Он также используется для оптического осаждения, что значительно улучшает оптическое качество. Фторид кобальта (II) доступен в большинстве объемов в составе сверхвысокой чистоты. Составы высокой чистоты улучшают оптические качества и их полезность в качестве стандарта.
Анализ
Для анализа этого соединения фторид кобальта (II) можно растворить в азотной кислоте. Затем раствор разбавляют водой до соответствующей концентрации для кобальта для спектрофотометрии AA или ICP . Небольшое количество соли можно растворить в холодной воде и проанализировать на фторид-ион с помощью фторид-селективного электрода или ионной хроматографии .
Химические свойства
CoF 2 - слабая кислота Льюиса . Комплексы кобальта (II) обычно бывают октаэдрическими или тетраэдрическими. Как 19-электронная разновидность, это хороший восстановитель, достаточно окисляемый до 18-электронного соединения. Фторид кобальта (II) можно восстановить водородом при 300 ° C.
Рекомендации
- ^ Pradyot Patnaik (2002), Справочник по неорганической химии , McGraw-Hill Professional, ISBN 978-0-07-049439-8
- ↑ Пашкевич, Д.С. Радченко С.М.; Мухортов Д.А., "Название статьи: Теплообмен между порошком фторида кобальта (II) и стенкой вращающегося цилиндра" (PDF) , Российский журнал прикладной химии , Бюро консультантов, ISSN 1070-4272 , архивировано с оригинала (PDF) 2004 г. -09-29 , извлекаются 2007-03-07
- ^ Эшкрофт / Мермин: Физика твердого тела (Табл. 33.2)
- ^ JC Bailar (1973), Комплексная неорганическая химия , Pergoamon

