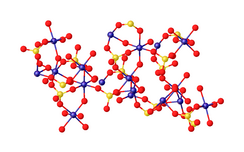
Сульфат хрома (III) - Chromium(III) sulfate

|
|
| Имена | |
|---|---|
|
Название ИЮПАК
Сульфат хрома (III)
|
|
| Другие имена
Основной сульфат хрома, сульфат хрома
|
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ЧЭБИ | |
| ChemSpider | |
| ECHA InfoCard |
100.030.217 |
| Номер ЕС | |
|
PubChem CID
|
|
| UNII | |
| Номер ООН | 2240 3077 |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Характеристики | |
| Cr 2 (SO 4 ) 3 • 12H 2 O | |
| Молярная масса | 392,16 г / моль 608,363 г / моль (додекагидрат) 716,45 г / моль (октадекагидрат) |
| Появление | красновато-коричневые кристаллы (безводные), пурпурные кристаллы (гидратированные) |
| Плотность | 3,10 г / см 3 (безводный) 1,86 г / см 3 (пентадекагидрат) 1,709 г / см 3 (октадекагидрат) |
| Температура плавления | 90 ° С |
| Точка кипения | > 700 ° C (разлагается до хромовой кислоты ) |
| нерастворимый (безводный) растворимый (гидратированный) |
|
| Растворимость | растворим в спирте, практически не растворим в кислоте |
| + 11,800 · 10 −6 см 3 / моль | |
| Опасности | |
| Паспорт безопасности | Паспорт безопасности |
| Пиктограммы GHS |
   
|
| Сигнальное слово GHS | Предупреждение |
| H314 , H317 , H332 , H334 , H335 , H340 , H350 , H373 , H412 | |
| Р201 , Р202 , Р260 , Р261 , Р264 , Р271 , P272 , P273 , P280 , P281 , P285 , P301 + 330 + 331 , P302 + 352 , P303 + 361 + 353 , Р304 + 312 , Р304 + 340 , Р304 + 341 , P305 + 351 + 338 , P308 + 313 , P310 , P312 , P314 , P321 , P333 + 313 , P342 + 311 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | Не воспламеняется |
| NIOSH (пределы воздействия на здоровье в США): | |
|
PEL (Допустимо)
|
TWA 1 мг / м 3 |
|
REL (рекомендуется)
|
TWA 0,5 мг / м 3 |
|
IDLH (Непосредственная опасность)
|
250 мг / м 3 |
| Родственные соединения | |
|
Другие катионы
|
Сульфат алюминия |
|
Связанные двойные соли
|
Хромовые квасцы |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Сульфат хрома (III) обычно относится к неорганическим соединениям с формулой Cr 2 (SO 4 ) 3 . x (H 2 O), где x может находиться в диапазоне от 0 до 18. Кроме того, известны плохо определенные, но коммерчески важные «основные сульфаты хрома». Эти соли обычно представляют собой твердые вещества фиолетового или зеленого цвета, растворимые в воде. Обычно используется при дублении кожи .
Сульфаты хрома (III)
Хорошо охарактеризованы три сульфата хрома (III):
- Безводный сульфат хрома (III) Cr 2 (SO 4 ) 3 (CAS # 10101-53-8) представляет собой твердое вещество фиолетового цвета, которое растворяется в воде при добавлении восстановителя, который образует сульфаты хрома (II).
- Гидратированный сульфат хрома (III), Cr 2 (SO 4 ) 3 · 18H 2 O, (CAS # 13520-66-6) представляет собой твердое вещество фиолетового цвета, которое легко растворяется в воде с образованием водного комплекса металла [Cr (H 2 O ) 6 ] 3+ . Формула этого соединения может быть записана более описательно как [Cr (H 2 O) 6 ] 2 (SO 4 ) 3 · 6H 2 O. Шесть из восемнадцати молекул воды в этой формульной единице представляют собой кристаллизационную воду .
- Гидратированный сульфат хрома (III) Cr 2 (SO 4 ) 3 · 15 (H 2 O) (CAS # 10031-37-5) представляет собой твердое вещество зеленого цвета, которое также легко растворяется в воде. Его получают нагреванием материала 18-гидрата выше 70 ° C. Дальнейшее нагревание дает безводный сульфат.
Известен ряд других сульфатов хрома (VI), но они также содержат гидроксидные или оксидные лиганды. Наиболее важным с коммерческой точки зрения является основной сульфат хрома , который, как считается, представляет собой [Cr 2 (H 2 O) 6 (OH) 4 ] SO 4 (CAS № 39380-78-4). Это результат частичной нейтрализации гексагидратов. Сообщалось о других гидроксидах хрома (III).
Производство
Наиболее полезным источником сульфата хрома (III) являются отходы Cr (III) от хроматного окисления различных органических соединений. Антрохинон и хинон производятся в больших масштабах путем обработки антрацена и фенола хромовой кислотой. Образуется побочный продукт оксида хрома (III), который легко экстрагируется серной кислотой. Выпаривание этих кислых растворов дает описанную выше гидратную соль. Гидратированные соли сульфата хрома также могут быть получены, хотя и неочищенные, путем экстракции различных других соединений хрома, но эти способы экономически нецелесообразны. Экстракция хромитовой руды серной кислотой в присутствии некоторого количества хромата дает растворы хрома (III ) сульфат, загрязненный ионами других металлов. Точно так же растворение хромовых сплавов дает сульфат хрома вместе с сульфатом железа.
Основной сульфат хрома (III)
Основной сульфат хрома получают из солей хромата восстановлением диоксидом серы , хотя существуют и другие методы. Формально сокращение можно было бы записать:
- Na 2 Cr 2 O 7 + 3 SO 2 + H 2 O → Cr 2 (SO 4 ) 3 + 2 NaOH
Так как 33% зарядов анионов связаны с гидроксильными ионами, основность составляет 33% (но на жаргоне дубильного материала она известна как пониженная на 33%). Продукты с более высокой степенью основности, например 42% или 50%, могут быть получены путем добавления карбоната натрия , они часто используются в сочетании с формиатом натрия . Сульфат натрия часто остается в техническом продукте, поскольку он инертен по отношению к процессу дубления. Важно полностью восстановить шестивалентный хром до трехвалентного, поскольку шестивалентный хром с большей вероятностью вызовет проблемы со здоровьем у дубильщиков и потребителей кожи.
Естественное явление
Чистый сульфат хрома (III), как в безводной, так и в водной форме, пока (2020 г.) неизвестен среди минеральных видов. Есть 3 комплексных минерала, частично являющиеся сульфатами Cr (III): бенторит , реддингтонит и птнизит .