Цементит - Cementite
| Стали |
|---|
 |
| Фазы |
| Микроструктуры |
| Классы |
| Другие материалы на основе железа |
Цементит (или карбид железа ) представляет собой соединение из железа и углерода , более точно промежуточного переходного металла карбида с формулой Fe 3 C. по весу, это 6,67% углерода и 93,3% железа. Он имеет ромбическую кристаллическую структуру. Это твердый, хрупкий материал, обычно классифицируемый как керамика в чистом виде, который часто встречается и является важным компонентом в черной металлургии . Хотя цементит присутствует в большинстве сталей и чугунов, он производится в качестве сырья в процессе карбида железа, который принадлежит к семейству альтернативных технологий производства чугуна. Название « цементит» возникло в результате исследований Флориса Осмонда и Дж. Верта, где структура затвердевшей стали теоретически представляет собой своего рода клеточную ткань с ферритом в качестве ядра и Fe 3 C в качестве оболочки клеток. Таким образом, карбид скрепил железо.
Металлургия
В системе железо-углерод (например, углеродистые стали и чугуны ) он является обычным компонентом, поскольку феррит может содержать не более 0,02 мас.% Несвязанного углерода. Следовательно, в углеродистых сталях и чугунах, которые медленно охлаждаются, часть углерода находится в форме цементита. Цементит образуется непосредственно из расплава в случае белого чугуна . В углеродистой стали цементит выделяется из аустенита, когда аустенит превращается в феррит при медленном охлаждении, или из мартенсита во время отпуска . Тесная смесь с ферритом, другим продуктом аустенита, образует пластинчатую структуру, называемую перлитом .
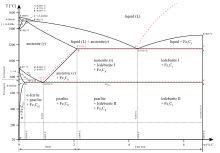
Хотя цементит термодинамически нестабилен и в конечном итоге превращается в аустенит (низкий уровень углерода) и графит (высокий уровень углерода) при более высоких температурах, он не разлагается при нагревании при температурах ниже температуры эвтектоида (723 ° C) на метастабильном железоуглеродистом состоянии. фазовая диаграмма.
Чистая форма
Цементит превращается из ферромагнитного в парамагнитный при температуре Кюри примерно 480 К.
Природный карбид железа (содержащий незначительное количество никеля и кобальта) встречается в железных метеоритах и называется когенитом в честь немецкого минералога Эмиля Коэна , который первым его описал. Поскольку углерод является одним из возможных второстепенных компонентов легких сплавов металлических ядер планет, свойства цементита (Fe 3 C) как простого заменителя когенита при высоких давлениях и температурах изучаются экспериментально. На рисунке показано поведение при сжатии при комнатной температуре.
Прочие карбиды железа
Существуют и другие формы метастабильных карбидов железа, которые были обнаружены в отпущенной стали и в промышленном процессе Фишера-Тропша . К ним относятся карбид эпсилон (ε) , гексагональный плотноупакованный Fe 2–3 C, выделения в углеродистых сталях с содержанием углерода> 0,2%, отпущенные при 100–200 ° C. Нестехиометрический ε-карбид растворяется при температуре выше ~ 200 ° C, при этом начинают образовываться карбиды Хегга и цементит. Карбид Хегга , моноклинный Fe 5 C 2 , выделяется в закаленных инструментальных сталях, отпущенных при 200–300 ° C. Он также был естественным образом обнаружен в виде минерала Эдскоттит в метеорите Веддерберн. Определение характеристик различных карбидов железа вовсе не является тривиальной задачей, и часто дифракция рентгеновских лучей дополняется мессбауэровской спектроскопией .
Рекомендации
Библиография
- Смит, Уильям Ф .; Хашеми, Джавад (2006). Основы материаловедения и инженерии (4-е изд.). Макгроу-Хилл. ISBN 978-0-07-295358-9.
- Дюран-Шарр, Мадлен (2004). Микроструктура сталей и чугунов . Springer. ISBN 978-3-642-05897-4.
-
Мессбауэровская спектроскопия карбидов железа: от прогноза к экспериментальному подтверждению

Внешние ссылки
- Кристаллическая структура цементита на НРЛ
- Хальштедт, Бенгт; Джурович, Деян; фон Аппен, Йорг; Dronskowski, Ричард; Дик, Алексей; Кёрманн, Фриц; Хикель, Тилманн; Нойгебауэр, Йорг (март 2010 г.). «Термодинамические свойства цементита (Fe 3 C)». Calphad . 34 (1): 129–133. DOI : 10.1016 / j.calphad.2010.01.004 .
- Le Caer, G .; Дюбуа, JM; Pijolat, M .; Perrichon, V .; Бюссьер, П. (ноябрь 1982 г.). «Характеристика с помощью мессбауэровской спектроскопии карбидов железа, образованных синтезом Фишера-Тропша». Журнал физической химии . 86 (24): 4799–4808. DOI : 10.1021 / j100221a030 .
- Bauer-Grosse, E .; Frantz, C .; Le Caer, G .; Хейман, Н. (июнь 1981 г.). «Образование метастабильных карбидов типа Fe 7 C 3 и Fe 5 C 2 во время кристаллизации аморфного сплава Fe 75 C 25 ». Журнал некристаллических твердых тел . 44 (2–3): 277–286. DOI : 10.1016 / 0022-3093 (81) 90030-2 .