Связь углерод – углерод - Carbon–carbon bond
Углерод-углеродную связь представляет собой ковалентную связь между двумя углеродными атомами . Наиболее распространенной формой является одинарная связь : связь, состоящая из двух электронов , по одному от каждого из двух атомов. Одинарная связь углерод-углерод является сигма-связью и образуется между одной гибридизированной орбиталью каждого из атомов углерода. В этане орбитали являются sp 3 - гибридизированными орбиталями, но одинарные связи, образованные между атомами углерода с другими гибридизациями, действительно возникают (например, sp 2 к sp 2 ). Фактически, атомы углерода в одинарной связи не обязательно должны иметь одинаковую гибридизацию. Атомы углерода также могут образовывать двойные связи в соединениях, называемых алкенами, или тройные связи в соединениях, называемых алкинами . Двойная связь образуется с sp 2 -гибридизованной орбиталью и p-орбиталью, которая не участвует в гибридизации. Тройная связь образуется с sp-гибридизированной орбиталью и двумя p-орбиталями от каждого атома. Использование p-орбиталей образует пи-связь .
Цепи и разветвления
Углерод - один из немногих элементов, которые могут образовывать длинные цепочки из собственных атомов - свойство, называемое катенацией . В сочетании с прочностью углеродно-углеродной связи это дает начало огромному количеству молекулярных форм, многие из которых являются важными структурными элементами жизни, поэтому у углеродных соединений есть своя собственная область изучения: органическая химия .
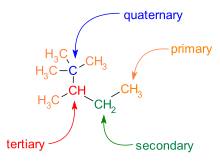
Ветвление также характерно для скелетов C − C. Атомы углерода в молекуле классифицируются по количеству углеродных соседей, которые у них есть:
- Первичный углерод имеет один сосед углерода.
- Вторичный углерод имеет два углеродных соседей.
- У третичного углерода есть три атома углерода.
- Четвертичный углерод имеет четыре углеродных соседей.
В «структурно сложных органических молекулах» именно трехмерная ориентация углерод-углеродных связей в четвертичных локусах определяет форму молекулы. Кроме того, четвертичные локусы обнаруживаются во многих биологически активных малых молекулах, таких как кортизон и морфин .
Синтез
Реакции образования углерод-углеродной связи - это органические реакции, в которых образуется новая углерод-углеродная связь. Они важны при производстве многих искусственных химикатов, таких как фармацевтические препараты и пластмассы .
Некоторые примеры реакций , которые образуют углерод-углеродные связи являются альдольной реакции , Дильса-Альдера , добавление реагента Гриньяра к карбонильной группе , в реакции Хека , в реакции Михаэля и реакции Виттига .
Направленный синтез желаемых трехмерных структур третичных углеродов был в значительной степени решен в конце 20- го века, но та же способность управлять четвертичным углеродным синтезом не начала проявляться до первого десятилетия 21- го века.
Прочность и длина склеивания
Одинарная связь углерод-углерод слабее, чем CH, OH, NH, HH, H-Cl, CF и многие двойные или тройные связи, и сравнима по прочности со связями CO, Si-O, PO и SH, но обычно считается сильным.
| Связь C – C | Молекула | Энергия диссоциации связи (ккал / моль) |
|---|---|---|
| СН 3 -СН 3 | этан | 90 |
| С 6 Н 5 -СН 3 | толуол | 102 |
| С 6 Н 5 -С 6 Н 5 | бифенил | 114 |
| СН 3 С (О) -СН 3 | ацетон | 84 |
| CH 3 -CN | ацетонитрил | 136 |
| СН 3 -СН 2 ОН | спирт этиловый | 88 |
Приведенные выше значения представляют энергии диссоциации связи CC, которые обычно встречаются; иногда выбросы могут резко отклоняться от этого диапазона.
| Молекула | Этан | Этилен | Ацетилен |
|---|---|---|---|
| Формула | С 2 Н 6 | С 2 Н 4 | С 2 Н 2 |
| Класс | алкан | алкен | алкин |
| Состав |

|

|

|
| Гибридизация углерода | sp 3 | sp 2 | зр |
| Длина CC облигации | 1,535 Å | 1,339 Å | 1,203 Å |
| Доля одинарной облигации СС | 100% | 87% | 78% |
| Метод определения структуры | микроволновая спектроскопия | микроволновая спектроскопия | ИК-спектроскопия |
Крайние случаи
Длинные, слабые одинарные связи CC
Были выявлены различные крайние случаи, когда связь CC удлинена. В димере Гомберга одна CC-связь довольно длинная и составляет 159,7 пикометров . Именно эта связь обратимо и легко разрывается при комнатной температуре в растворе:
В еще более загруженной молекуле гексакис (3,5-ди- трет- бутилфенил) этана энергия диссоциации связи с образованием стабилизированного триарилметильного радикала составляет всего 8 ккал / моль. Гексакис (3,5-ди- трет- бутилфенил) этан также является следствием серьезной стерической перегрузки и имеет сильно вытянутую центральную связь длиной 167 мкм.
Скрученные, слабые двойные связи CC
Структура тетракис (диметиламино) этилена (ТДАЭ) сильно искажена. Двугранный угол для два Н 2 концов С 28º , хотя С = С расстоянием нормально 135 мкм. Почти изоструктурный тетраизопропилэтилен также имеет расстояние C = C 135 мкм, но его ядро C 6 является плоским.
Короткие, прочные тройные облигации СС
С другой стороны, центральная одинарная связь углерод-углерод диацетилена очень сильна при 160 ккал / моль, поскольку одинарная связь соединяет два атома углерода в результате sp-гибридизации. Множественные связи углерод-углерод обычно прочнее; двойная связь этилена и тройная связь ацетилена имеют энергии диссоциации связи 174 и 230 ккал / моль соответственно. Очень короткая тройная связь 115 пм наблюдалась для разновидностей иодония [HC≡C – I + Ph] [CF 3 SO 3 - ] из-за сильно электроноакцепторного иодониевого фрагмента.