Правило Бента - Bent's rule
В химии, правило Бент описывает и объясняет взаимосвязь между орбитальной гибридизации центральных атомов в молекулах и электроотрицательности из заместителей . Правило было сформулировано Генри А. Бентом следующим образом:
Характер атома концентрируется на орбиталях, направленных к электроположительным заместителям.
Химическая структура из молекулы тесно связана с его свойствами и реакционной способностью . Теория валентной связи предполагает, что молекулярные структуры обусловлены ковалентными связями между атомами и что каждая связь состоит из двух перекрывающихся и обычно гибридизированных атомных орбиталей . Традиционно предполагается , что p-блочные элементы в молекулах гибридизуются строго как sp n , где n равно 1, 2 или 3. Кроме того, предполагается, что все гибридные орбитали эквивалентны (т. Е. N + 1 sp n орбитали имеют тот же символ p). Результаты этого подхода обычно хороши, но их можно улучшить, допустив изовалентную гибридизацию , при которой гибридизированные орбитали могут иметь нецелочисленный и неравный p-характер. Правило Бента дает качественную оценку того, как должны быть построены эти гибридизированные орбитали. Правило Бента состоит в том, что в молекуле центральный атом, связанный с несколькими группами, будет гибридизоваться, так что орбитали с более s-характером направлены к электроположительным группам, в то время как орбитали с более p-характером будут направлены к более электроотрицательным группам. Удалив предположение о том, что все гибридные орбитали являются эквивалентными sp n- орбиталями, можно получить более точные прогнозы и объяснения таких свойств, как геометрия молекул и прочность связи. Правило Бента было предложено в качестве альтернативы теории VSEPR в качестве элементарного объяснения наблюдаемой молекулярной геометрии простых молекул с преимуществами более легкого согласования с современными теориями связывания и более сильного экспериментального подтверждения.
Справедливость правила Бента для 75 типов связей между основными элементами группы была исследована недавно. Для связей с более крупными атомами из более низких периодов тенденции орбитальной гибридизации сильно зависят как от электроотрицательности, так и от размера орбиты.
История
В начале 1930-х годов, вскоре после начального развития квантовой механики , эти теории начали применяться к молекулярной структуре Полингом , Слейтером , Колсоном и другими. В частности, Полинг ввел концепцию гибридизации , в которой атомные s- и p-орбитали объединяются, чтобы получить гибридные sp, sp 2 и sp 3 орбитали. Гибридные орбитали оказались мощными в объяснении молекулярной геометрии простых молекул, таких как метан (тетраэдрические с sp 3 углеродом). Однако небольшие отклонения от этой идеальной геометрии стали очевидны в 1940-х годах. Особенно хорошо известен пример воды , где угол между атомами водорода составляет 104,5 °, что намного меньше ожидаемых 109,5 °. Чтобы объяснить такие несоответствия, было высказано предположение, что гибридизация может приводить к орбиталям с неодинаковым s- и p-характером. А.Д. Уолш описал в 1947 году взаимосвязь между электроотрицательностью групп, связанных с углеродом, и гибридизацией указанного углерода. Наконец, в 1961 году Бент опубликовал крупный обзор литературы, посвященной молекулярной структуре, гибридизации центрального атома и электроотрицательности заместителей, и именно для этой работы правило Бента получило свое название.
Обоснование

Полярные ковалентные связи
Неформальное обоснование правила Бента основывается на том, что s-орбитали имеют меньшую энергию, чем p-орбитали. Связи между элементами с разной электроотрицательностью будут полярными, и электронная плотность в таких связях будет смещена в сторону более электроотрицательного элемента. Применение этого к молекуле фторметана демонстрирует правило Бента. Поскольку углерод более электроотрицателен, чем водород, электронная плотность в связях CH будет ближе к углеродной. Энергия этих электронов будет сильно зависеть от гибридных орбиталей, которые углерод вносит в эти связи из-за повышенной электронной плотности около углерода. Увеличивая количество s-символов на этих гибридных орбиталях, можно уменьшить энергию этих электронов, потому что s-орбитали меньше по энергии, чем p-орбитали.
По той же логике и тому факту, что фтор более электроотрицателен, чем углерод, электронная плотность в связи CF будет ближе к фтору. Гибридная орбиталь, которую углерод вносит в связь CF, будет иметь относительно меньшую электронную плотность, чем в случае CH, и поэтому энергия этой связи будет меньше зависеть от гибридизации углерода. Направляя гибридные орбитали с более p-характером к фтору, энергия этой связи не очень сильно увеличивается.
Вместо того, чтобы направлять эквивалентные sp 3 -орбитали ко всем четырем заместителям, смещение s-символа в сторону связей CH значительно стабилизирует эти связи из-за повышенной электронной плотности около углерода, в то время как смещение s-символа от связи CF увеличит ее энергию на меньшую величину. количество, потому что электронная плотность этой связи дальше от углерода. Характер атома на атоме углерода был направлен в сторону более электроположительных водородных заместителей и далек от электроотрицательного фтора, что и предполагает правило Бента.
Хотя фторметан является особым случаем, приведенный выше аргумент может быть применен к любой структуре с центральным атомом и 2 или более заместителями. Ключевым моментом является то, что концентрация атома на орбиталях, направленных к электроположительным заместителям, за счет его истощения на орбиталях, направленных на электроотрицательные заместители, приводит к общему снижению энергии системы. Этот стабилизирующий компромисс ответственен за правило Бента.
Несвязывающие орбитали
Правило Бента может быть расширено, чтобы рационализировать гибридизацию несвязывающих орбиталей. С одной стороны, неподеленную пару (занятую несвязывающую орбиталь) можно рассматривать как предельный случай электроположительного заместителя с электронной плотностью, полностью поляризованной по направлению к центральному атому. Правило Бента предсказывает, что для стабилизации неподеленных, тесно удерживаемых несвязывающих электронов орбитали неподеленных пар должны принимать высокий s-характер . С другой стороны, незанятая несвязывающая орбиталь может рассматриваться как предельный случай электроотрицательного заместителя с электронной плотностью, полностью поляризованной по направлению к лиганду. Правило Бента предсказывает, что для того, чтобы оставить как можно больше s-символа для оставшихся занятых орбиталей, незанятые несвязывающие орбитали должны максимизировать p-характер .
Экспериментально первый вывод согласуется с уменьшенными валентными углами молекул с неподеленными парами, такими как вода или аммиак, по сравнению с метаном, в то время как второй вывод согласуется с плоской структурой молекул с незанятыми несвязывающими орбиталями, такими как мономерный боран и ионы карбения.
Последствия
Правило Бента можно использовать для объяснения тенденций как в молекулярной структуре, так и в реакционной способности. После определения того, как гибридизация центрального атома должна влиять на конкретное свойство, можно исследовать электроотрицательность заместителей, чтобы увидеть, выполняется ли правило Бента.
Углы скрепления
Знание углов между связями - важный компонент в определении молекулярной структуры. В теории валентных связей предполагается, что ковалентные связи состоят из двух электронов, лежащих на перекрывающихся, обычно гибридизованных, атомных орбиталях связанных атомов. Орбитальная гибридизация объясняет, например, почему метан является тетраэдрическим, а этилен - плоским. Однако есть отклонения от идеальной геометрии sp n- гибридизации, например, в воде и аммиаке . Валентные углы в этих молекулах составляют 104,5 ° и 107 ° соответственно, что ниже ожидаемого тетраэдрического угла 109,5 °. Традиционный подход к объяснению этих различий - теория VSEPR . В этой структуре предполагается, что валентные электроны находятся в локализованных областях, и предполагается, что неподеленные пары отталкивают друг друга в большей степени, чем связывающие пары.
Правило Бента дает альтернативное объяснение того, почему некоторые валентные углы отличаются от идеальной геометрии. Во-первых, тенденция между гибридизацией центрального атома и валентным углом может быть определена с использованием модельных соединений метана , этилена и ацетилена . По порядку атомы углерода направляют sp 3 , sp 2 и sp орбитали к водородным заместителям. Валентные углы между заместителями составляют ~ 109,5 °, ~ 120 ° и 180 °. Эта простая система демонстрирует, что гибридизированные атомные орбитали с более высоким значением p будут иметь меньший угол между собой. Этот результат можно сделать строгим и количественным, как теорему Коулсона (см. Раздел «Формальная теория» ниже).
Теперь, когда связь между гибридизацией и валентными углами установлена, правило Бента можно применить к конкретным примерам. Следующее было использовано в оригинальной статье Бента, которая считает, что групповая электроотрицательность метильной группы меньше, чем у атома водорода, потому что замещение метила снижает кислотные константы диссоциации муравьиной кислоты и уксусной кислоты.
| Молекула | Угол связи между заместителями |
|---|---|
|
Диметиловый эфир |
111 ° |
|
Метанол |
107-109 ° |
|
Воды |
104,5 ° |
|
Дифторид кислорода |
103,8 ° |
По мере продвижения по таблице заместители становятся более электроотрицательными, и угол связи между ними уменьшается. Согласно правилу Бента, по мере увеличения электроотрицательности заместителей орбитали с большим р-характером будут направлены к этим группам. Согласно приведенному выше обсуждению, это уменьшит угол связи. Это согласуется с экспериментальными результатами. Сравнивая это объяснение с теорией VSEPR , VSEPR не может объяснить, почему угол в диметиловом эфире больше 109,5 °.
При прогнозировании угла связи воды, правило Бента предполагает, что гибридные орбитали с более s-характером должны быть направлены к неподеленным парам, в то время как это оставляет орбитали с более p-характером, направленными к атомам водорода, что приводит к отклонению от идеализированного O (sp 3 ) -гибрида. орбитали с символом 25% s и символом 75% p. В случае воды с ее углом НОН 104,5 ° связывающие орбитали ОН построены из орбиталей O (~ sp 4,0 ) (~ 20% s, ~ 80% p), в то время как неподеленные пары состоят из O (~ sp 2,3 ) орбитали (~ 30% s, ~ 70% p). Как обсуждалось в приведенном выше обосновании, неподеленные пары ведут себя как очень электроположительные заместители и имеют характер избытка s. В результате связывающие электроны имеют повышенный р-характер. Этот увеличенный p-характер в этих орбиталях уменьшает валентный угол между ними до менее чем тетраэдрический 109,5 °. Та же логика может быть применена к аммиаку (угол связи HNH 107,0 °, с тремя N (~ sp 3,4 или 23% s) связывающими орбиталями и одной неподеленной парой N (~ sp 2,1 или 32% s)), другой канонический пример этот феномен.
Та же тенденция сохраняется и для азотсодержащих соединений. Вопреки ожиданиям теории VSEPR, но в соответствии с правилом Бента, валентные углы аммиака (NH 3 ) и трифторида азота (NF 3 ) составляют 107 ° и 102 ° соответственно.
В отличие от теории VSEPR , теоретические основы которой сейчас кажутся шаткими, правило Бента по-прежнему считается важным принципом в современных методах лечения связывания. Например, модификация этого анализа все еще жизнеспособна, даже если неподеленные пары H 2 O считаются неэквивалентными в силу их симметрии (т. Е. Только s, а плоские кислородные АО p x и p y гибридизуются. чтобы сформировать две связывающие ОН орбитали σ O-H и неподеленную пару n O (σ) , в то время как p z становится неэквивалентной чистой p-символьной неподеленной парой n O (π) ), как в случае неподеленных пар, возникающих из методов естественной связи орбиталей .
Длина скрепления
Подобно валентным углам, гибридизация атома может быть связана с длиной образующихся связей. По мере увеличения s-характера связывающих орбиталей длина s-связи уменьшается.
| Молекула | Средняя длина углерод-углеродной связи |
|---|---|
 |
1,54 Å |
 |
1,50 Å |
 |
1,46 Å |
Добавляя электроотрицательные заместители и изменяя гибридизацию центральных атомов, можно изменять длину связи. Если молекула содержит структуру XA - Y, замена заместителя X на более электроотрицательный атом изменяет гибридизацию центрального атома A и укорачивает соседнюю связь A - Y.
| Молекула | Средняя длина связи углерод – фтор |
|---|---|
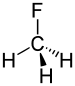 Фторметан |
1,388 Å |
 Дифторметан |
1,358 Å |
 Трифторметан |
1,329 Å |
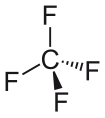 Тетрафторметан |
1,323 Å |
Поскольку фтор гораздо более электроотрицателен, чем водород, во фторметане углерод будет направлять гибридные орбитали с более высоким s-характером к трем атомам водорода, чем к фтору. В дифторметане есть только два атома водорода, поэтому меньше всего s-характера направлено к ним, а больше направлено к двум фторам, что укорачивает длину связи C-F по сравнению с фторметаном. Эта тенденция сохраняется вплоть до тетрафторметана, связи CF которого имеют наивысший s-характер (25%) и наименьшую длину связи в ряду.
Та же тенденция сохраняется и для хлорированных аналогов метана, хотя эффект менее драматичен, поскольку хлор менее электроотрицателен, чем фтор.
| Молекула | Средняя длина связи углерод-хлор |
|---|---|
 Хлорметан |
1,783 Å |
 Дихлорметан |
1,772 Å |
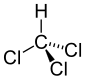 Трихлорметан |
1,767 Å |
 Тетрахлорметан |
1,766 Å |
Вышеупомянутые случаи, кажется, демонстрируют, что размер хлора менее важен, чем его электроотрицательность. Прогноз, основанный только на стерических принципах, привел бы к противоположной тенденции, поскольку большие заместители хлора были бы более предпочтительными при большом расстоянии друг от друга. Поскольку стерическое объяснение противоречит экспериментальному результату, правило Бента, вероятно, играет главную роль в определении структуры.
J CH Константы взаимодействия
Возможно, наиболее прямым измерением s-характера на связывающей орбитали между водородом и углеродом являются константы взаимодействия 1 H- 13 C, определенные из спектров ЯМР . Теория предсказывает, что значения J CH будут намного выше в связях с более s-характером. В частности, константа связи одной связи 13 C- 1 H 1 J 13C-1H связана с дробным s-характером углеродной гибридной орбитали, используемой для образования связи, посредством эмпирической зависимости . (Например, чистая гибридная атомная орбиталь sp 3, обнаруженная в связи CH метана, будет иметь характер 25% s, что приведет к ожидаемой константе связи 500 Гц × 0,25 = 125 Гц, что отлично согласуется с экспериментально определенным значением.)
| Молекула | J CH (метильных протонов) |
|---|---|
 Метан |
125 Гц |
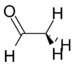 Ацетальдегид |
127 Гц |
 1,1,1-Трихлорэтан |
134 Гц |
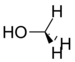 Метанол |
141 Гц |
 Фторметан |
149 Гц |
По мере увеличения электроотрицательности заместителя количество р-символа, направленного в сторону заместителя, также увеличивается. Это оставляет более s-характер связи с протонами метила, что приводит к увеличению констант взаимодействия J CH .
Индуктивный эффект
Индуктивный эффект можно объяснить с правилом Бента. Индуктивный эффект - это передача заряда через ковалентные связи, и правило Бента обеспечивает механизм для таких результатов через различия в гибридизации. В приведенной ниже таблице, когда группы, связанные с центральным углеродом, становятся более электроотрицательными, центральный углерод становится более электроноакцепторным, что измеряется константой полярного заместителя . Константы полярных заместителей в принципе аналогичны значениям σ из уравнения Хаммета , поскольку возрастающее значение соответствует большей способности акцептировать электроны. Правило Бента предполагает, что по мере увеличения электроотрицательности групп больше p-символа отклоняется в сторону этих групп, что оставляет больше s-символа в связи между центральным углеродом и R-группой. Поскольку s-орбитали имеют большую электронную плотность ближе к ядру, чем p-орбитали, электронная плотность в связи C-R будет больше смещаться в сторону углерода по мере увеличения s-символа. Это сделает центральный углерод более отталкивающим электроны для группы R. Таким образом, электроноакцепторная способность заместителей была передана соседнему углероду, что и предсказывает индукционный эффект.
| Заместитель |
Константа полярного заместителя (большие значения означают большую способность акцептора электронов) |
|---|---|
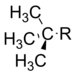 т –бутил |
−0,30 |
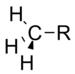 Метил |
0,00 |
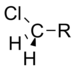 Хлорметил |
1.05 |
 Дихлорметил |
1,94 |
 Трихлорметил |
2,65 |
Формальная теория
Правило Бента обеспечивает дополнительный уровень точности теории валентных связей . Теория валентных связей предполагает, что ковалентные связи состоят из двух электронов, лежащих на перекрывающихся, обычно гибридизованных, атомных орбиталях двух связывающих атомов. Предположение о том, что ковалентная связь представляет собой линейную комбинацию атомных орбиталей только двух связывающих атомов, является приближением (см. Теорию молекулярных орбиталей ), но теория валентной связи достаточно точна, чтобы иметь и продолжает оказывать большое влияние на то, как связь понимается.
В теории валентной связи каждый из двух атомов вносит свой вклад в атомную орбиталь, а электроны в перекрывающихся орбитали образуют ковалентную связь. Атомы обычно не вносят в связи чистую водородоподобную орбиталь . Если бы атомы могли вносить только водородоподобные орбитали, то экспериментально подтвержденная тетраэдрическая структура метана была бы невозможна, поскольку 2s и 2p орбитали углерода не имеют такой геометрии. Это и другие противоречия привели к предложению орбитальной гибридизации . В этой структуре атомные орбитали могут смешиваться, чтобы произвести эквивалентное количество орбиталей различных форм и энергий. В вышеупомянутом случае метана 2s и три 2p-орбитали углерода гибридизуются с получением четырех эквивалентных sp 3 -орбиталей, что устраняет структурное несоответствие. Орбитальная гибридизация позволила теории валентных связей успешно объяснить геометрию и свойства огромного числа молекул.
В традиционной теории гибридизации все гибридные орбитали эквивалентны. А именно, атомные s- и p-орбитали объединяются, чтобы дать четыре sp i 3 = 1 ⁄ √ 4 ( s + √ 3 p i ) орбитали, три sp i 2 = 1 ⁄ √ 3 ( s + √ 2 p i ). орбитали, или две sp i = 1 ⁄ √ 2 ( s + p i ) орбитали. Эти комбинации выбраны для удовлетворения двух условий. Во-первых, общее количество s- и p-орбитальных вкладов должно быть эквивалентным до и после гибридизации. Во-вторых, гибридные орбитали должны быть ортогональны друг другу. Если бы две гибридные орбитали не были ортогональными, по определению они имели бы ненулевое перекрытие орбиталей. Электроны на этих орбиталях будут взаимодействовать, и если бы одна из этих орбиталей была вовлечена в ковалентную связь, другая орбиталь также имела бы ненулевое взаимодействие с этой связью, нарушая принцип теории валентных связей два электрона на связь.
Чтобы построить гибридные s- и p-орбитали, пусть первая гибридная орбиталь задается как s + √ λ i p i , где p i направлено к связывающей группе, а λ i определяет количество p-характера, которое имеет эта гибридная орбиталь. Это взвешенная сумма волновых функций. Теперь выберите вторую гибридную орбиталь s + √ λ j p j , где p j каким-то образом направлено, а λ j - количество символов p на этой второй орбите. Значение λ j и направление p j должны быть определены так, чтобы результирующая орбиталь могла быть нормализована и чтобы она была ортогональна первой гибридной орбитали. Гибрид, безусловно, можно нормализовать, поскольку он представляет собой сумму двух нормализованных волновых функций. Ортогональность должна быть установлена так, чтобы две гибридные орбитали могли быть вовлечены в отдельные ковалентные связи. Скалярное произведение ортогональных орбиталей должны быть равны нулю , и вычисления скалярного произведения построенных гибридов дает расчет следующий.
S орбитали нормализуется и поэтому скалярное произведение ⟨ S | с ⟩ = 1 . Кроме того, орбиталь s ортогональна орбиталям p i и p j , что приводит к двум членам в приведенном выше примере, равным нулю. Наконец, последний член является внутренним произведением двух нормированных функций, расположенных под углом ω ij друг к другу, что по определению дает cos ω ij . Однако ортогональность связывающих орбиталей требует, чтобы 1 + √ λ i λ j cos ω ij = 0 , поэтому в результате мы получаем теорему Коулсона:
Это означает, что четыре атомных орбитали s и p могут быть гибридизированы в произвольных направлениях при условии, что все коэффициенты λ попарно удовлетворяют вышеуказанному условию, чтобы гарантировать, что результирующие орбитали ортогональны.
Правило Бента, согласно которому центральные атомы направляют орбитали с большим p-характером в сторону более электроотрицательных заместителей, легко применимо к вышесказанному, если отметить, что увеличение коэффициента λ i увеличивает p-характер гибридной орбитали s + √ λ i p i . Таким образом, если центральный атом А связан с двумя группами Х и Y , а Y является более электроотрицательным , чем X, то А будет гибридизоваться так , что λ Х < Х Y . Для точного предсказания геометрии молекул, исходя из первых принципов, необходимы более сложные теоретические и вычислительные методы, выходящие за рамки правила Бента, но правило Бента обеспечивает превосходную эвристику для объяснения молекулярных структур.
Смотрите также
- Молекулярная орбитальная теория
- Орбитальная гибридизация
- Молекулярная геометрия
- Линейная комбинация атомных орбиталей




![{\ displaystyle {\ begin {align} \ left \ langle s + {\ sqrt {\ lambda _ {i}}} p_ {i} {\ Big \ vert} s + {\ sqrt {\ lambda _ {j}}} p_ {j} \ right \ rangle & = \ langle s \ mid s \ rangle + {\ sqrt {\ lambda _ {i}}} \ langle s \ mid p_ {i} \ rangle + {\ sqrt {\ lambda _ { j}}} \ langle s \ mid p_ {j} \ rangle + {\ sqrt {\ lambda _ {i} \ lambda _ {j}}} \ langle p_ {i} \ mid p_ {j} \ rangle \\ [4pt] & = 1 + 0 + 0 + {\ sqrt {\ lambda _ {i} \ lambda _ {j}}} \ cos \ omega _ {ij} = 1 + {\ sqrt {\ lambda _ {i} \ lambda _ {j}}} \ cos \ omega _ {ij} \ конец {выровнено}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a9a0eccf9438e2d82c4e98622999feded965adac)
