Пероксид бария - Barium peroxide

|
|
|
|
| Имена | |
|---|---|
|
Название ИЮПАК
перекись бария
|
|
| Другие имена
Двуокись
бария, двуокись бария |
|
| Идентификаторы | |
|
3D модель ( JSmol )
|
|
| ChemSpider | |
| ECHA InfoCard | 100.013.754 |
| Номер ЕС | |
|
PubChem CID
|
|
| Номер RTECS | |
| UNII | |
| Номер ООН | 1449 |
|
Панель управления CompTox ( EPA )
|
|
|
|
|
|
| Свойства | |
| BaO 2 | |
| Молярная масса | 169,33 г / моль (безводный) 313,45 (октагидрат) |
| Внешность | Серо-белое кристаллическое (безводное) бесцветное твердое вещество (октагидрат) |
| Запах | без запаха |
| Плотность | 5,68 г / см 3 (безводный) 2,292 г / см 3 (октагидрат) |
| Температура плавления | 450 ° С (842 ° F, 723 К) |
| Точка кипения | 800 ° C (1470 ° F; 1070 K) (разлагается на BaO & O 2. ) |
|
безводный 0,091 г / 100 мл (20 ° C) октагидрата 0,168 г / см 3 |
|
| Растворимость | растворяется с разложением в кислоте |
| -40,6 · 10 −6 см 3 / моль | |
| Структура | |
| Тетрагональный | |
| D 17 4h , I4 / ммм, tI6 | |
| 6 | |
| Опасности | |
| Пиктограммы GHS |
 
|
| Сигнальное слово GHS | Предупреждение |
| H272 , H302 , H332 | |
| Р210 , Р220 , P221 , P261 , P264 , P270 , P271 , P280 , P301 + 312 , Р304 + 312 , Р304 + 340 , P312 , P330 , P370 + 378 , P501 | |
| NFPA 704 (огненный алмаз) | |
|
Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). |
|
|
|
|
| Ссылки на инфобоксы | |
Пероксид бария представляет собой неорганическое соединение с формулой Ba O 2 . Это белое твердое вещество (когда нечистота становится серым) является одним из наиболее распространенных неорганических пероксидов и первым обнаруженным пероксидным соединением. Являясь окислителем и при возгорании дает ярко-зеленый цвет (как и все соединения бария), он находит некоторое применение в фейерверках ; исторически он также использовался в качестве прекурсора перекиси водорода .
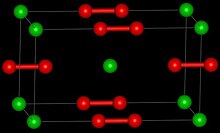
Структура
Пероксид бария - это пероксид, содержащий O2-
2субъединицы. Твердое вещество изоморфными с карбидом кальция , CaC 2 .
Приготовление и использование
Пероксид бария образуется в результате обратимой реакции O 2 с оксидом бария . Пероксид образует около 500 ° C, а кислород выделяется при температуре выше 820 ° C.
- 2 BaO + O 2 ⇌ 2 BaO 2
Эта реакция является основой устаревшего процесса Брина для отделения кислорода от атмосферы. Другие оксиды, например Na 2 O и SrO, ведут себя аналогичным образом.
В другом устаревшем применении пероксид бария когда-то использовался для производства пероксида водорода в результате его реакции с серной кислотой:
- BaO 2 + H 2 SO 4 → H 2 O 2 + BaSO 4
Нерастворимый сульфат бария отфильтровывают из смеси.
Сноски
- ^ a b Размещение избытка кислорода в монооксидах группы II - SC Middleburgh, RW Grimes и KPD Lagerlof Journal Американского керамического общества, 2013 г., том 96, страницы 308–311. DOI : 10.1111 / j.1551-2916.2012.05452.x
- ^ Массалимов, ИА; Киреева М.С. Сангалов, Ю. А. (2002). «Структура и свойства механически активированного пероксида бария». Неорганические материалы . 38 (4): 363–366. DOI : 10,1023 / A: 1015105922260 .
- ^ a b Харальд Якоб; Стефан Лейнингер; Томас Леманн; Сильвия Якоби; Свен Гутеворт. «Пероксосоединения неорганические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. DOI : 10.1002 / 14356007.a19_177.pub2 .
- ^ Holleman, AF; Виберг, Э. "Неорганическая химия" Academic Press: Сан-Диего, 2001. ISBN 0-12-352651-5 .

